ΕΡΓΑΣΤΗΡΙΟ ΦΥΣΙΚΗΣ
Μελέτη της χρονικής εξέλιξης
των θερμοκρασιών
Δυο υγρών σε θερμική αλληλεπίδραση
Σκοποι:
· η διαπίστωση της μεταβίβασης ενέργειας από ένα σύστημα σε ένα άλλο, με θερμότητα
· η παρακολούθηση της πορείας ενός απομονωμένου συστήματος, προς την κατάσταση της θερμικής ισορροπίας
· η προέκταση των συμπερασμάτων του πειράματος, σε φαινόμενα θερμικών ισορροπιών που συμβαίνουν καθημερινά
Απαραιτητα Οργανα
·
δοχείο Α με θερμομονωμένα
τοιχώματα πολύ μικρής θερμοχωρητικότητας (θερμιδόμετρο) και καπάκι που έχει
υποδοχές σε κατάλληλες θέσεις για δύο θερμόμετρα
·
δοχείο Β με λεπτά θερμικά αγώγιμα τοιχώματα(π.χ.
αλουμίνιο), που έχει ύψος λίγο μικρότερο από το δοχείο Α και διάμετρο αρκετά
μικρότερη από αυτό έτσι ώστε να τοποθετείται μέσα του
·
δυο θερμόμετρα με κλίμακες –10 έως +100 0C (ενδεικτικά)
·
χρονόμετρο
·
δοχείο ζέσεως νερού
·
ογκομετρικό δοχείο
·
γκαζάκι, τρίποδας και
πλέγμα
Απαραιτητεσ Γνωσεισ
Η ενέργεια μπορεί να μεταβιβάζεται από ένα σύστημα σε ένα άλλο με δύο τρόπους. Ο ένας είναι με το έργο της δύναμης και ο άλλος με θερμότητα.
Στην περίπτωση που σε ένα δοχείο Α υπάρχει νερό μάζας m1 και θερμοκρασίας θ1 και μέσα σε αυτό τοποθετήσουμε ένα άλλο δοχείο Β με μεταλλικά τοιχώματα που περιέχει νερό μάζας m2 και θερμοκρασίας θ2, γνωρίζουμε ότι μετά από λίγο τα δύο υγρά θα έχουν την ίδια θερμοκρασία θ. Ενέργεια μεταβιβάστηκε , με θερμότητα, από το δοχείο που περιείχε νερό με μεγαλύτερη θερμοκρασία στο δοχείο που περιείχε νερό με μικρότερη θερμοκρασία. Στο τέλος η κοινή θερμοκρασία θ θα είναι μεταξύ των θερμοκρασιών θ1 και θ2.
Επειδή κατά τη θερμική αλληλεπίδραση δεν παρατηρείται καμία μεταφορά ενέργειας με έργο, και το σύστημα των δύο δοχείων είναι θερμικά απομονωμένο από το περιβάλλον του, μπορούμε να γράψουμε:
0 + ΔUολ = 0
δηλαδή ΔU1 + ΔU 2 + ΔUA + ΔUB = 0.
Όμως είναι ΔU1 = m1c(θ-θ1), ΔU2 = m2c(θ–θ2), ΔUA = KA(θ-θ1) και ΔUB = KB(θ-θ2). Οι ποσότητες KA και KB είναι οι θερμοχωρητικότητες των δοχείων Α και Β και δίδονται από τον κατασκευαστή. Μπορούμε λοιπόν να υπολογίσουμε την τελική θερμοκρασία θ που θα έχουν και οι δύο ποσότητες του νερού των δοχείων Α και Β αν γνωρίζουμε επίσης τις θερμοκρασίες θ1 και θ2 καθώς και τις ποσότητες του νερού των δύο δοχείων από την εξίσωση:
m1c(θ-θ1) + m2c(θ–θ2) + KA(θ-θ1) + KB(θ-θ2) = 0
Η ειδική θερμότητα του νερού είναι γνωστή c = 1 cal/grgrad.
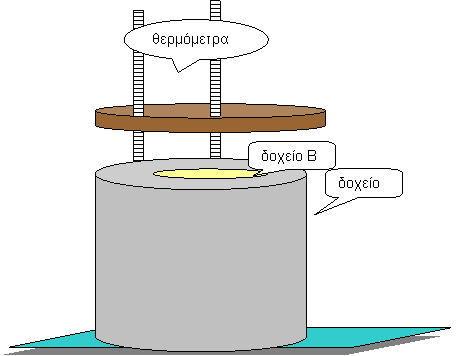
Η πειραματική διάταξη
Τοποθετούμε το δοχείο Β μέσα στο δοχείο Α και συμπληρώνουμε το χώρο μεταξύ των δύο δοχείων με νερό που έχει θερμοκρασία περιβάλλοντος. Μέσα στο δοχείο Β θα ρίξουμε το νερό που έχουμε προηγουμένως θερμάνει. Πρέπει επίσης να τοποθετήσουμε τα θερμόμετρα στις ειδικές υποδοχές του καπακιού του δοχείου Α και να προσέξουμε ώστε ο υδράργυρος να είναι αρκετά βυθισμένος στο νερό των δοχείων καθώς επίσης η θερμοκρασία περιβάλλοντος (χαμηλή) να διαβάζεται καθαρά.
Διαδικασια Εργασιασ
1. Τοποθετήστε το δοχείο Β μέσα στο Α και συμπληρώστε με νερό από τη βρύση, το χώρο μεταξύ των δύο δοχείων. Μετρήστε και καταγράψτε την αρχική θερμοκρασία του νερού.
2. Προσθέσατε αρκετό νερό στο δοχείο ζέσεως και τοποθετήστε το πάνω στο πλέγμα του τρίποδα. Στη συνέχεια ανάψτε το γκαζάκι και ζεστάνετε το νερό. Μια θερμοκρασία 60 0C είναι αρκετή.
3. Βγάλτε το δοχείο Β από το λουτρό του και γεμίστε το με ζεστό νερό. Μετρήστε την αρχική θερμοκρασία.
4. Ένας μαθητής της ομάδας πρέπει να είναι έτοιμος με το χρονόμετρο στο χέρι, ώστε μόλις ακολουθήσει το επόμενο βήμα να αρχίσει ταυτόχρονα και η χρονομέτρηση. Ένας άλλος μαθητής της ομάδας θα συμπληρώνει τον πίνακα του τετραδίου την κατάλληλη χρονική στιγμή.
5. Στη συνέχεια τοποθετήστε το δοχείο Β μέσα στο δοχείο Α και προσαρμόστε το καπάκι με τα θερμόμετρα, κλείνοντας και απομονώνοντας ταυτόχρονα το σύστημα από το περιβάλλον του. Τώρα αρχίζει η χρονική καταγραφή της θερμικής εξέλιξης του φαινομένου.
6. Αρχικά να καταγράφετε τις ενδείξεις των δυο θερμομέτρων κάθε μισό λεπτό αν αυτό είναι δυνατόν. Στη συνέχεια κάθε ένα λεπτό. Πάρτε αρκετές μετρήσεις.
7. Από τα στοιχεία του πίνακα ΠΚ – 1 κάντε σε κοινούς άξονες τη γραφική παράσταση θερμοκρασία – χρόνος.
8. Ποια θερμοκρασία προκύπτει για τη θερμική ισορροπία, από το προηγούμενο διάγραμμα;
9. Με βάση όσα έχουμε αναφέρει στις απαραίτητες γνώσεις, να υπολογίστε θεωρητικά τη θερμοκρασία κατά τη θερμική ισορροπία. Αν δεν έχετε όλα τα στοιχεία που απαιτούνται για τον υπολογισμό, θεωρήστε αμελητέες τις θερμοχωρητικότητες των δοχείων Α και Β.
10. Συγκρίνατε την πειραματική και τη θεωρητική θερμοκρασία κατά τη θερμική ισορροπία.
11. Παρατηρώντας το διάγραμμα που κατασκευάσατε μπορείτε να πείτε ποια στιγμή έχουμε πρακτικά θερμική ισορροπία;
12. Μετά τη θερμική ισορροπία γιατί η θερμοκρασία του συστήματος δεν παραμένει σταθερή;
13. Βασιζόμενοι στη γραφική παράσταση που κατασκευάσατε πειραματικά μπορείτε να εκτιμήσετε σε πόση ώρα από τη στιγμή που πρακτικά έχουμε θερμική ισορροπία, το σύστημα θα έχει 5 0C μικρότερη θερμοκρασία;