1 / 20
- Από τα διαλύματα α)
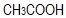 0,1 M, β)
0,1 M, β) 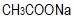 0,1 M, γ)
0,1 M, γ) 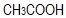 0,2 M και NaOH 0,1M και δ)
0,2 M και NaOH 0,1M και δ) 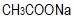 0,2 M υψηλότερο pH στην ίδια θερμοκρασία εμφανίζει ...
0,2 M υψηλότερο pH στην ίδια θερμοκρασία εμφανίζει ...- το γ.
- το δ.
- το α.
- το β.
- Όταν αραιώνουμε ένα υδατικό διάλυμα
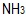 υπό σταθερή θερμοκρασία, τότε αυξάνεται:
υπό σταθερή θερμοκρασία, τότε αυξάνεται:- η συγκέντρωση των OH-
- το pH του διαλύματος
- ο βαθμός ιοντισμού της
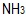
- η σταθερά ιοντισμού της
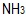
- Η τιμή της σταθεράς αυτοϊοντισμού του νερού
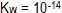 στους
στους 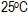 ισχύει στην ίδια θερμοκρασία ...
ισχύει στην ίδια θερμοκρασία ...- μόνο στο καθαρό νερό
- μόνο σε διαλύματα οξέων ή βάσεων
- σε όλα τα υδατικά διαλύματα
- σε όλα τα διαλύματα
- Η τιμή της σταθερά ιοντισμού ενός ασθενούς οξέος ΗΑ σ’ ένα υδατικό του διάλυμα εξαρτάται από ...
- από το pH του διαλύματος
- το αν υπάρχει επίδραση κοινού ιόντος
- τη θερμοκρασία
- τη συγκέντρωση του ΗΑ
- Όταν υδατικό διάλυμα ασθενούς ηλεκτρολύτη αραιώνεται με νερό, σε σταθερή θερμοκρασία τότε ...
- το pH του διαλύματος πάντοτε μειώνεται
- η σταθερά ιοντισμού του ηλεκτρολύτη μειώνεται.
- η συγκέντρωση του ηλεκτρολύτη στο διάλυμα αυξάνεται
- ο βαθμός ιοντισμού του ηλεκτρολύτη αυξάνεται.
- Σε θερμοκρασία θ το pH του καθαρού νερού είναι ίσο με 7,2. Επομένως:
- θ = 25 C
- θ < 25 C
- θ > 25 C
- Σε V1 mL διαλύματος
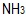 0,1 M προσθέτουμε V2 mL διαλύματος HCl 0,1 M. To διάλυμα που προκύπτει έχει pH = 10. Άρα:
0,1 M προσθέτουμε V2 mL διαλύματος HCl 0,1 M. To διάλυμα που προκύπτει έχει pH = 10. Άρα:- δεν μπορούμε να γνωρίζουμε
-
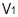 <
< 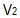
-
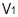 >
> 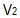
-
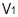 =
= 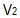
- Από τα οξέα α)
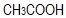 , β)
, β) 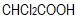 , γ)
, γ) 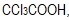 και δ)
και δ) 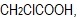 ισχυρότερο είναι το...
ισχυρότερο είναι το...- α
- δ
- γ
- β
- Συζηγές οξύ του υδροξυλίου είναι το ...
- οξώνιο
- νερό
- ιόν οξυγόνου
- Η ιοντική ισορροπία HI +
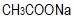

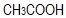 + NaI είναι μετατοπισμένη ...
+ NaI είναι μετατοπισμένη ...- προς τα αριστερά
- προς τα δεξιά
- είτε προς τα δεξιά είτε προς τα αριστερά ανάλογα τις συνθήκες
- Για το pH διαλύματος
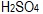 συγκέντρωσης 0,01 M ισχύει ...
συγκέντρωσης 0,01 M ισχύει ...- 1 < pH < 2
- pH = 2
- pH = 1
- 3 > pH > 2
- Υδατικό διάλυμα HCl (Δ1) και υδατικό διάλυμα
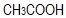 (Δ2) έχουν τον ίδιο όγκο και την ίδια τιμή pH. Τότε για την πλήρη εξουδετέρωση τους ...
(Δ2) έχουν τον ίδιο όγκο και την ίδια τιμή pH. Τότε για την πλήρη εξουδετέρωση τους ...- και Δ1 και Δ2 απαιτούν ίσα mol NaOH
- απαιτεί περισσότερα mol NaOH το Δ2
- απαιτεί περισσότερα mol NaOH το Δ1
- Το σημείο στο οποίο παρατηρείται από τον πειραματιστή η αλλαγή στο χρώμα του ογκομετρούμενου διαλύματος ονομάζεται ...
- τελικό σημείο
- ουδέτερο σημείο
- σημείο μεταπτώσεως
- ισοδύναμο σημείο
- Αν το οξύ
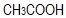 έχει σταθερά ιοντικής ισορροπίας
έχει σταθερά ιοντικής ισορροπίας 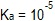 τότε για τη συζυγή του βάση θα ισχύει στην ίδια θερμοκρασία ...
τότε για τη συζυγή του βάση θα ισχύει στην ίδια θερμοκρασία ...-
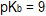
-
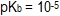
- pH = 9
- pOH = 9
-
- Ουσία η οποία ιοντίζεται πλήρως στο νερό, όταν διαλυθεί σε συγκέντρωση 0,1 Μ σε αυτό είναι το ...
- υπερχλωρικό οξύ
- μεθανικό οξύ
- υδροξείδιο του νατρίου
- χλωριούχο αμμώνιο
- Διάλυμα
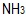 ογκομετρείται με πρότυπο διάλυμα HCl. Στο ισοδύναμο σημείο της ογκομέτρησης ισχύει:
ογκομετρείται με πρότυπο διάλυμα HCl. Στο ισοδύναμο σημείο της ογκομέτρησης ισχύει:- pH = 7
- το pH εξαρτάται από την συγκέντρωση της
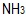
- pH > 7
- pH < 7
- Σε όγκο V υδατικού διαλύματος της ασθενούς βάσεως Β 0,1Μ για να αυξηθεί η τιμή του pH πρέπει να προσθέσουμε ...
- όγκο V διαλύματος της
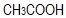 0,1Μ
0,1Μ - όγκο V διαλύματος Β 0,1Μ
- όγκο V διαλύματος HCl 0,1Μ
- όγκο V διαλύματος Β 0,3Μ
- όγκο V διαλύματος της
- Αν διαλύσουμε HCl σε υδατικό διάλυμα
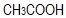 (ασθενές οξύ) τότε ...
(ασθενές οξύ) τότε ...- η
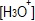 ] αυξάνεται, ενώ η
] αυξάνεται, ενώ η 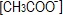 μειώνεται
μειώνεται - η
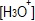 αυξάνεται, ενώ η
αυξάνεται, ενώ η 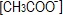 δε μεταβάλλεται.
δε μεταβάλλεται. - οι
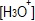 και
και 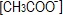 αυξάνονται
αυξάνονται - η
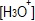 μειώνεται, ενώ η
μειώνεται, ενώ η 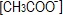 αυξάνεται
αυξάνεται
- η
- Κατάλληλος δείκτης για την ογκομέτρηση άγνωστης συγκέντρωσης διαλύματος
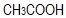 με πρότυπο διάλυμα NaOH είναι ...
με πρότυπο διάλυμα NaOH είναι ...- η φαινολοφθαλεΐνη
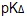 =8,5
=8,5 - κίτρινο αλιζαρίνης
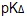 =12
=12 - το πορτοκαλί του μεθυλίου
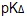 =3,5
=3,5 - η βρωμοκρεσόλη
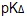 =4,5
=4,5
- η φαινολοφθαλεΐνη
- Θα παρασκευάσουμε ρυθμιστικό διάλυμα αν σε 100 mL διαλύματος NaOH 0,1 Μ προσθέσουμε ...
- 100 mL διαλύματος
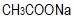 0,2 M
0,2 M - 100 mL διαλύματος
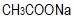 0,1 M
0,1 M - 100 mL διαλύματος
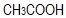 0,2 M
0,2 M - 100 mL διαλύματος
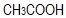 0,1 M
0,1 M
- 100 mL διαλύματος