Θα έχετε παρατηρήσει, στις ετικέτες των αντιδραστηρίων που υπάρχουν στο σχολείο σας πολλά άλατα σε μορφή κρυστάλλων εμφανίζονται να ενσωματώνουν στο μόριό τους μόρια νερού σε σταθερή μοριακή αναλογία. Τα άλατα αυτά χαρακτηρίζονται ως «ένυδρα» και το νερό που περιέχεται στους κρυστάλλους ονομάζεται «νερό κρυστάλλωσης». Πχ το ένυδρο χλωριούχο βάριο εμφανίζεται με χημικό τύπο: BaCl2• 2 H2O. Τα μόρια του νερού κρυστάλλωσης καταλαμβάνουν καθορισμένες θέσεις στο πλέγμα του κρυστάλλου ή απλά συμπληρώνουν κενά που υπάρχουν στο πλέγμα. Οι δυνάμεις που συγκρατούν τα μόρια του νερού στον κρύσταλλο είναι διάφορων κατηγοριών όπως δεσμοί υδρογόνου, ηλεκτροστατικές έλξεις κλπ. Τα μόρια αυτά του νερού μπορούν να απομακρυνθούν τις περισσότερες φορές με θέρμανση
Απαιτούμενα όργανα και υλικά
| Δοκιμαστικός σωλήνας θερμάντοχος | Μίγμα από BaCl2•2H2O και CuSO4•5H2O |
| ζυγός ακριβείας 0,1 g | |
| ορθοστάτης | |
| σύνδεσμος, λαβίδα | |
| λύχνος Bunsen | |
| χαρτί ζύγισης | |
| κουταλάκι | |
| αανπτήρας |
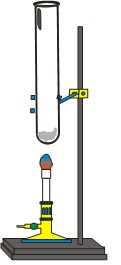
Πορεία του πειράματος

_____________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________
Αν χρησιμοποιηθεί φούρνος μικροκυμάτων θέτετε το δείγμα σε αυτόν και θερμαίνετε για 20 min. Ζυγίζετε και επαναλαμβάνετε από εκεί και πέρα την διαδικασία κάθε 5 min μέχρι να σταθεροποιηθεί η ζυγιζόμενη μάζα.