|
Ορισμοί
Τα οξειδωτικά μέσα ή απλά οξειδωτικά είναι ουσίες (άτομα, μόρια, ιόντα) που μπορούν να προκαλέσουν την οξείδωση άλλων χημικών ουσιών. Ως οξειδωτικά μπορούν να δράσουν ουσίες οι οποίες περιέχουν άτομα που μπορούν να αναχθούν, δηλαδή να ελαττώσουν τον αριθμό οξείδωσης τους. Επoμένως, ως οξειδωτικά μπορούν να δράσουν:
- Tα ισχυρά ηλεκτραρνητικά στοιχεία (F2, O3, Cl2, Br2, Ο2), αποσπώντας ένα ή δύο ηλεκτρόνια από την ουσία που οξειδώνουν.
- Ενώσεις ή ιόντα που περιέχουν ένα στοιχείο με το μεγαλύτερο (ή έναν από τους μεγαλύτερους) αριθμό οξείδωσής του, π.χ.:
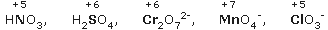
Τα αναγωγικά μέσα ή απλά αναγωγικά είναι ουσίες (άτομα, μόρια, ιόντα) που μπορούν να προκαλέσουν την αναγωγή άλλων χημικών ουσιών. Ως αναγωγικά μπορούν να δράσουν ουσίες οι οποίες περιέχουν άτομα που μπορούν να οξειδωθούν, δηλαδή να αυξήσουν τον αριθμό οξείδωσής τους. Έτσι, ως αναγωγικά μπορούν να δράσουν:
- Τα δραστικά μέταλλα, που ως ηλεκτροθετικά στοιχεία αποβάλλουν εύκολα ηλεκτρόνια.
- Ο άνθρακας, το υδρογόνο και ορισμένα υδρίδια μετάλλων (NaH, CaH2, LiAlH4).
- Ενώσεις ή ιόντα που περιέχουν ένα στοιχείο με το μικρότερο (ή έναν από τους μικρότερους) αριθμό οξείδωσής του, π.χ:
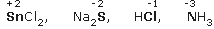
|
Για παράδειγμα από τις ανόργανες ενώσεις του αζώτου:
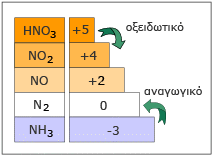
- το πυκνό και το αραιό νιτρικό οξύ, κατά τη μετατροπή τους αντίστοιχα σε διοξείδιο και μονοξείδιο του αζώτου, δρουν ως οξειδωτικά, επειδή και στις δύο περιπτώσεις το άζωτο ελαττώνει από +5 σε +4 και +2 αντίστοιχα τον αριθμό οξείδωσής του, δηλαδή να ανάγεται.
- η αμμωνία κατά τη μετατροπή της σε στοιχειακό άζωτο δρα ως αναγωγικό, επειδή το άζωτο αυξάνει από -3 σε 0 τον αριθμό οξείδωσής του, δηλαδή οξειδώνεται.
|
Σχήμα: Αριθμοί οξείδωσης του αζώτου σε διάφορες ενώσεις του. |
Παρατηρήσεις
1. Στην περίπτωση των οξειδοαναγωγικών αντιδράσεων μεταφοράς ηλεκτρονίων, η ισχύς των
οξειδωτικών και των αναγωγικών μέσων εκφράζεται ποσοτικά από το πρότυπο δυναμικό.
2. Το κατά πόσο μία ουσία θα δράσει ως οξειδωτικό ή ως αναγωγικό εξαρτάται και από το με ποια
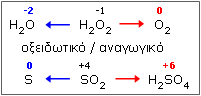
ουσία αντιδρά. Έτσι, τα Η2Ο2 και SO2:
- παρουσία ενός ισχυρότερου οξειδωτικού, όπως π.χ. τα ιόντα MnO4-, μπορούν να οξειδωθούν αντίστοιχα προς οξυγόνο και θειικό οξύ και να δράσουν ως αναγωγικά
- παρουσία ενός ισχυρότερου αναγωγικού, όπως π.χ. το ΗΙ, μπορούν να αναχθούν προς νερό και στοιχειακό θείο αντίστοιχα και να δράσουν ως οξειδωτικά.
|
|
| |
3. Σε ορισμένες πάλι περιπτώσεις, η συμπεριφορά ενός οξειδωτικού ή αναγωγικού μέσου μπορεί να
επηρεάζεται από το περιβάλλον στο οποίο βρίσκεται. Έτσι:
- τα νιτρικά ιόντα, ΝΟ3-, παρουσία
πυκνού νιτρικού οξέος μετατρέπονται σε διοξείδιο του αζώτου, ενώ παρουσία αραιού νιτρικού οξέος μετατρέπονται σε μονοξείδιο του αζώτου
- η συμπεριφορά των υπερμαγγανικών ιόντων (MnO4-) ως οξειδωτικού εξαρτάται από την οξύτητα του διαλύματος. Τα ιόντα αυτά, που τα διαλύματά τους έχουν ένα χαρακτηριστικό σκούρο πορφυρό χρώμα (4), μετατρέπονται:
|
- Σε όξινα διαλύματα, σε άχρωμα κατιόντα Mn2+, οπότε το διάλυμα αποχρωματίζεται.
- Σε ουδέτερα ή ελαφρώς βασικά διαλύματα, σε στερεό MnO2 καστανού χρώματος.
- Σε περισσότερο βασικά διαλύματα, σε ανιόντα MnO42-, που δίνουν στο διάλυμα ένα χαρακτηριστικό πράσινο χρώμα.
|
| |
|