

- ΟΞΕΙΔΟΑΝΑΓΩΓΗ
- Εισαγωγή
- Αριθμός οξείδωσης
- Οξείδωση-Αναγωγή
- Οξειδωτικά-Αναγωγικά
- Ημιαντιδράσεις οξείδωσης-αναγωγής
- Αντιδράσεις οξειδοαναγωγής με τη μέθοδο ημιαντιδράσεων
- ΙΔΙΟΤΗΤΕΣ ΜΕΤΑΛΛΩΝ-ΑΓΩΓΟΙ
- Εισαγωγή
- Δομή μεταλλικού πλέγματος
- Δραστικότητα μετάλλων
- Ηλεκτροδιαλυτική τάση μετάλλων
- Ηλεκτρικοί αγωγοί
- ΓΑΛΒΑΝΙΚΑ ΣΤΟΙΧΕΙΑ
- Εισαγωγή
- Γαλβανικά στοιχεία
- Ημιστοιχεία-Ε ημιστοιχείων
- Ε0 ημιστοιχείων
- Γέφυρα άλατος
- Συμβολισμός ημιστοιχείου-Ηλεκτρόδια ημιστοιχείων
- Συμβολισμός γαλβανικού στοιχείου
- Ε στοιχείου - Ε0 στοιχείου-Υπολογισμοί Ε0
- Γραφή συνολικής αντίδρασης στοιχείου
- Παραδείγματα γραφής στοιχείων
- ΔG οξειδοαναγωγικής αντίδρασης
- Εξίσωση Nerst
- Παραδείγματα χρήσης εξίσωσης Nerst
- Εφαρμογές στοιχείων -Μπαταρίες
- ΠΕΙΡΑΜΑ - Στοιχείο Daniell
- ΗΛΕΚΤΡΟΛΥΣΗ
- Ηλεκτρολυτικά στοιχεία
- Προϊόντα ηλεκτρόλυσης
- Σύγκριση γαλβανικού – ηλεκτρολυτικού στοιχείου
- Παραδείγματα ηλεκτρόλυσης
- Νόμοι Faraday
- ΠΕΙΡΑΜΑ - Ηλεκτρόλυση Η2Ο ή αρ.δ. H2SO4
2.1 Ιδιότητες των μετάλλων – Εισαγωγή
Τα μέταλλα βρίσκονται στη φύση ελεύθερα (αυτοφυή) ή και ενωμένα. Τα δραστικά μέταλλα των ομάδων ΙΑ, ΙΙΑ, ΙΙΙΑ, (Na, K, Mg, Ca, Ba, Ra, Al…..) βρίσκονται μόνο ενωμένα.
Τα πιο ευγενή ( π.χ. Cu, Hg, Ag, Bi…..) βρίσκονται και αυτοφυή και ενωμένα με τη μορφή διαφόρων ορυκτών.
Τα μέταλλα έχουν χαρακτηριστικές φυσικές και χημικές ιδιότητες. Τα στοιχειώδη σωματίδια από τα οποία αποτελούνται είναι ενωμένα με έναν ειδικό τύπο δεσμού, το λεγόμενο μεταλλικό δεσμό στον οποίο οφείλεται και ο μεταλλικός τους χαρακτήρας.
Γενικά τα μέταλλα έχουν την τάση να δίνουν ηλεκτρόνια και να μετατρέπονται σε θετικά ιόντα (κατιόντα). Όσο μεγαλύτερη είναι αυτή η τάση, τόσο πιο ηλεκτροθετικό χαρακτηρίζεται το μέταλλο ή αλλιώς τόσο πιο αναγωγικό είναι (προκαλεί αναγωγή ενώ το ίδιο οξειδώνεται).
Η τάση αυτή φαίνεται από την ηλεκτροχημική σειρά των μετάλλων.
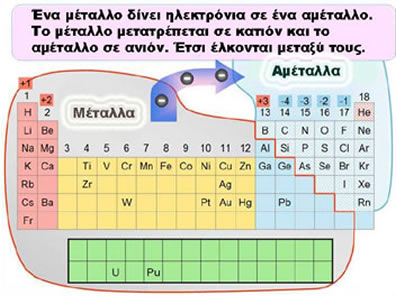
Οι θέσεις των μετάλλων και των αμετάλλων στον περιοδικό πίνακα
|